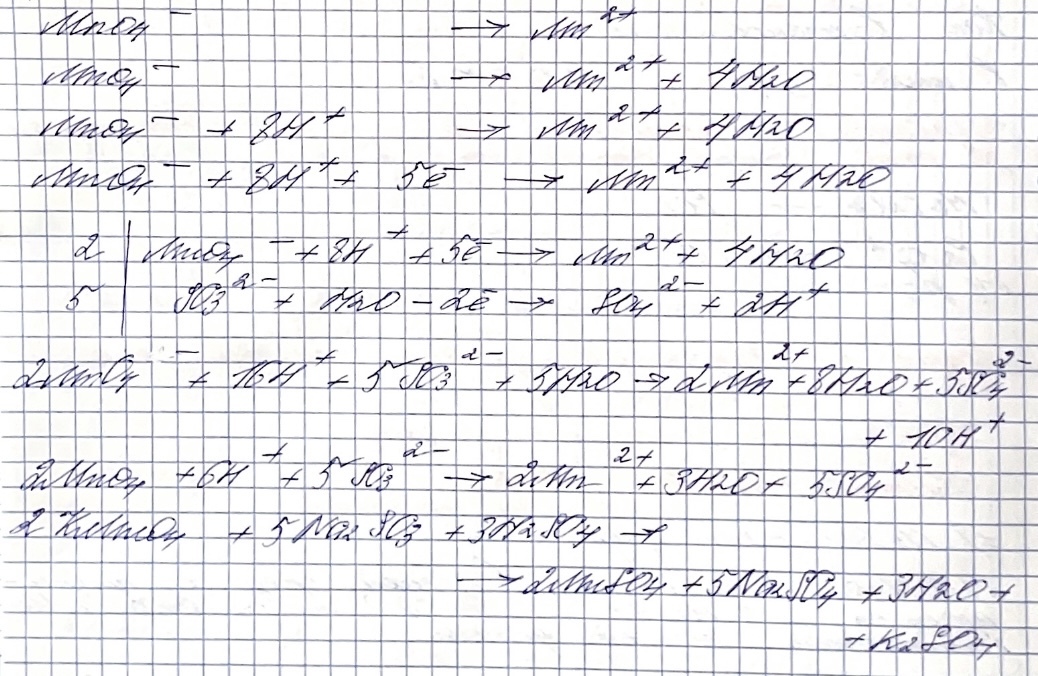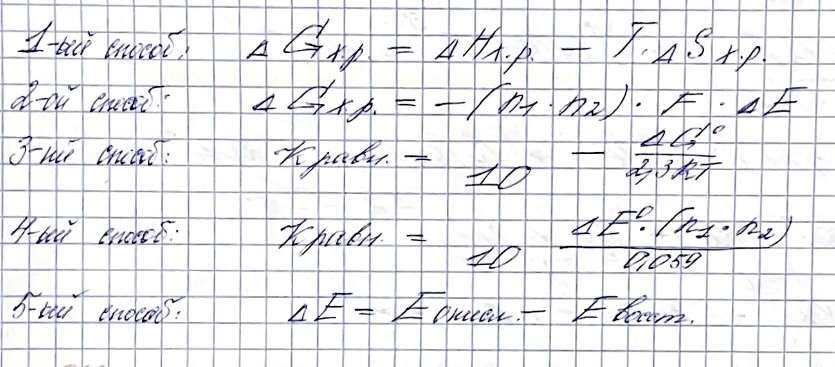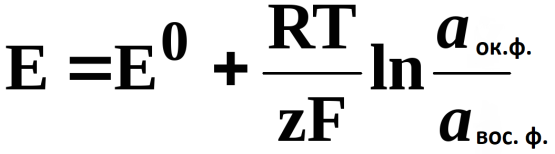В нейтральной и слабокислой среде:
I2 (коричневый раствор)→ 2I- (бесцветный раствор)
В щелочной среде йод разрушается:
I2 + NaOH(комнатная температура) → NaI+ NaIO+ H2O
(нагревание) →NaI +NaIO3 + H2O
Тиосульфат натрия – восстановитель за счет атома S в минимальной степени окисления -2
В нейтральной среде:
Na2S2O3 (бесцветный раствор)→ Na2S4O6 (тетратионат натрия)
Метамышьяковая кислота и метаарсенаты – восстановители за счет As в степени окисления +3
HAsO2→H3AsO4(ортомышьяковистая кислота)
AsO2- (бесцветный раствор) →H2AsO4- (дигидроарсенат ион, бесцветный раствор)
Пероксиды – и окислители, и восстановители за счет О в промежуточной степени окисления -1
Как окислитель:
В кислой среде H2O2→H2O
В щелочной средеH2O2→OH-
Как восстановитель:
В любой среде H2O→O2
Щавелевая кислота и оксалаты – восстановители за счет С в степени окисления +3
H2C2O4 → CO2
C2O42- (бесцветный раствор) → CO2
Перманганат калия – окислитель за счет Mn в максимальной степени окисления +7
В сильнокислой среде KMnO4 (красно-фиолетовый) → Mn2+ (бесцветный раствор)
В сильнощелочной среде →K2MnO4- (изумрудно-зеленый раствор)
В слабокислой, слабощелочной, нейтральной среде →MnO2↓ (бурый осадок)
Некоторые правила составления ОВР в водном растворе
Правило №1
В кислой среде в ту сторону полуреакции, где не хватает атомов О, ставят столько же молекул Н2О. В другую сторону полуреакции – удвоенное количество Н+.
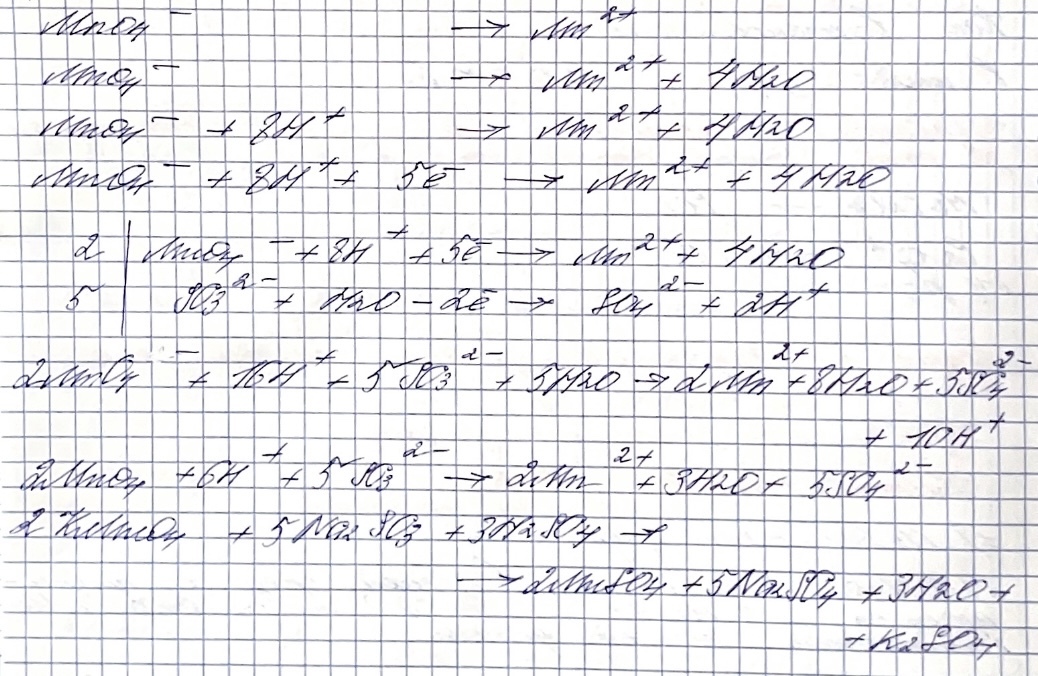
Правило №2
В щелочной среде в ту сторону полуреакции, где избыток атомов О, ставят столько же молекул Н2О. В другую сторону полуреакции – удвоенное количество ОН-.
Правило №3
В щелочной среде в ту сторону полуреакции, где избыток атомов Н, ставят столько же ОН- групп. В другую сторону полуреакции добавляют столько же Н2О.

Требования к титранту и ОВР
1. Полнота протекания ОВР
ΔЕ = Е окислителя – Е восстановителя ≥ 0,2В
2. Желательно, чтобы титрант был сильным окислителем

3. Титрант не должен вступать в побочные реакции
4. Высокая скорость реакции
- большинство ОВР идут медленнее КОР
- многостадийность восстановления
Mn+7 → Mn+6 → Mn+4 → Mn+3→ Mn+2
- ↑ скорость: ↑t до 60-70 градусов (добавить катализатор MnSO4)
5. Наличие способа фиксирования КТТ
- перманганатометрия в кислой среде – безиндикаторное титрование (бесцветный → розовый)
- дихроматометрическое титрование: на фоне зеленого расвтора нужно увидеть лишнюю каплю оранжевого цвета. Нереально. Используют дифениламин: синий → зеленый. Йод с крахмалом образует прочный комплекс, индикатор добавляют только в конце титрования.
Оценка полноты протекания ОВР
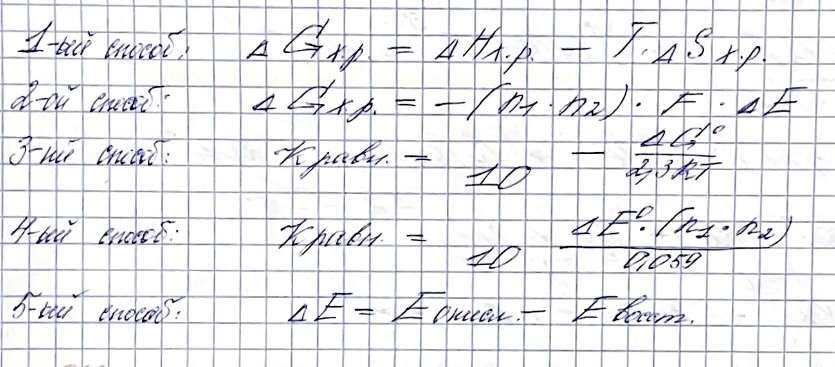
Окислительно-восстановительный потенциал системы. Факторы, влияющие на него.
ОВП – это потенциал окислительно-восстановительной системы, измеренный относительно стандартного водородного электрода.
Уравнение Нернста
· Для концентрированного раствора:
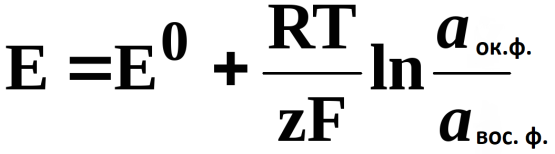
· Для разбавленного раствора:
- при любой температуре

- при 298 К=25°С

Факторы, влияющие на ОВП
1. Природа данной системы.
2. Концентрация ок.ф., в.ф., их отношение.
3. Температура
4. Кислотность раствора (рН, рОН)
5. Комплексообразование с участием одного из ионов
6. Осаждение с участием одного из ионов.