Сырьем для производства аммиака является азотоводородная смесь (АВС) стехиометрического состава N2:H2 = 1:3. В некоторых схемах синтеза аммиака не требуется выделять азот из воздуха в чистом виде: воздух дозируют в газовую смесь для достижения стехиометрического соотношения N2:H2 = 1:3. В других схемах используют и чистый жидкий азот для тонкой очистки синтез-газа от вредных примесей, и газообразный, вводя его в строго корректируемом соотношении в конвертированный газ. В последнем случае воздух подвергают разделению методом глубокого охлаждения. Так как ресурсы атмосферного азота практически неисчерпаемы, сырьевая база аммиачного производства определяется вторым компонентом смеси – водородом, который может быть получен разделением обратного коксового газа, газификацией твердого топлива, конверсией природного газа.

Основное значение имеют методы конверсии метана и окиси углерода, а также разделение коксового газа.
Разделение коксового газа
В коксовом газе содержится большое количество водорода. Его выделяют охлаждением системы до -190 0С., при этом практически полностью конденсируются газовые примеси. Давление в системе от 1,5 до 2,0 МПа, что облегчает конденсацию.
После очистки от сероводорода газ сжимают, нафталиновым маслом удаляют ароматические примеси. Щелочью и аммиаком связывают остатки H2Sи CO2.
Оставшуюся смесь нагревают до 200 0С и пропускают над катализатором гидрирования (палладий на оксиде алюминия). Этилен превращается в этан.
Полученную смесь охлаждают до -40 0С, при этом вымораживается вода и бензол.
Последовательно охлаждают до -110, -145, -190 0С, вымораживаются этилен, пропилен и метан.
Затем газ поступает в испаритель жидкого азота, где при температуре -190 0С промывают оставшуюся смесь от угарного газа и метана жидким азотом. В смеси остается водород.
Конверсия природного газа
Метод основан на действии окислителей.
При недостатке кислорода протекает кислородная конверсия до CO2. Образующуюся смесь нагревают при температуре 850 -900 0С на никелево-алюминиевом катализаторе:
CH4 + 0,5O2 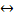 2H2 +СО
2H2 +СО
CH4 + 2O2 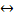 2H2О +СО2
2H2О +СО2
Затем происходит паровая конверсия, часть метана взаимодействует с CO2 с образованием CO и O2:
CH4 + CO2 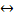 2CO + 2H2
2CO + 2H2
Далее систему охлаждают до 200-250 0С, протекает реакция CO + H2O 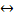 CO2 + H2,и образовавшийся CO2 возвращается в процесс.
CO2 + H2,и образовавшийся CO2 возвращается в процесс.
При паровой конверсии угарного газа при уменьшении температуры равновесие смещается к H2. Используется трехкратный избыток водяного пара.
Полученная АВС содержит каталитические яды: обратимые (O2, CO и CO2) и необратимые (соединения серы и фосфора). Для очистки проводят абсорбцию мокрым методом и сухим.
Для тонкой очистки используют хемосорбцию обычно с жидкими реагентами с последующим гидрированием примесей или промывкой системы жидким азотом.
Окончательная очистка достигается каталитическим гидрированием (метанированием) при температуре 250-3000С, давлении 30МПа, на никелево-алюминиевом катализаторе.
CO + H2 = CH4 + H2O
CO2 + 4H2 = CH4 + 2H2O
O2 + 2H2 = 2H2O
Если данный процесс проводить на этой стадии, то уже может образоваться аммиак.
Выделяющееся на данной стадии тепло используется в схеме производства аммиака.




 2H2 +СО
2H2 +СО


