При зарядке:
Анод (положительный электрод):
LiCoO2- xē → Li1-xCoO2 + xLi+
Катод (отрицательный электрод):
С + xLi+ + xē → CLix
При разрядке:
Анод (отрицательный электрод):
CLix – xē → С + xLi+
Катод (положительный электрод):
Li1-xCoO2 + xLi++ xē → LiCoO2
Электролиз. Количественные расчеты с использованием законов Фарадея.
Электролиз — это совокупность окислительно-восстановительных процессов под действием внешнего источника постоянного тока в специальных устройствах — электролизерах. При электролизе происходит направленное перемещение ионов электролита, окисление на аноде одних из них и восстановление на катоде — других. Однако в этом случае катодом служит отрицательно заряженный электрод, а анодом — положительно заряженный, (при электролизе вещества восстанавливаются на катоде и окисляются на аноде).
В качестве примера рассмотрим электролиз расплава хлорида натрия, диссоциирующего по схеме:
NaCl ↔ Na + +CI-
При пропускании электрического тока через расплав катионы натрия движутся к катоду. Здесь, взаимодействуя с электронами из внешней цепи, они восстанавливаются:
Na+ + е = Na
Анионы хлора перемещаются к аноду, где отдают избыточные электроны и окисляются:
Cl - - е = Cl c последующим образованием молекул газа Cl2
Каждая из этих полуреакций протекает не самопроизвольно, а за счет энергии внешнего источника. Суммарная окислительно-восстановительная реакция описывается уравнением:
Na+ + 2CI- = Na + Cl2
Количественно электролиз описывается двумя законами М. Фарадея (1827):
1. Масса выделившегося на электроде вещества пропорциональна количеству электричества, прошедшего через электролит.
2. Одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные их химическим эквивалентам.
Из второго закона следует, что для выделения одного моля химических эквивалентов вещества следует затратить одно и то же количество электричества, не зависящее ни от каких условий. Измерениями установлено, что это количество составляет 96485 (округленно 96500) кулонов и называется постоянной Фарадея (F). Следовательно:

Умножив обе части уравнения на молярную массу эквивалентов, получим:
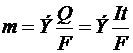
где: m — масса вещества, г; I — сила тока, А; t — продолжительность электролиза, с; Э — молярная масса эквивалентов вещества, г/моль экв.
38. Гальванопластика и гальваностегия как примеры технического использования электролиза.
Гальванопластика - электрохимический способ копирования (получение точных копий изделий). Широко используется в технике при изготовлении матриц в полиграфии, пресс-форм для прессования грампластинок и т.п. Этим способом изготовляют металлические сетки, ювелирные изделия, копии скульптур, гравюр, детали сложной конфигурации. Способ отличается исключительно высокой точностью воспроизведения рельефа изделия.
Гальваностегия - электрохимический процесс покрытия одного металла другим, более устойчивым в механическом и химическом отношении, например, стальные детали покрывают хромом, никелем; медные - никелем, серебром или другими металлами.
для гальваностегических покрытий используют многие металлы и сплавы (серебро, цинк, олово, никель, медь, хром и их сплавы), в гальванопластике обычно применяют лишь отложения меди, никеля и серебра