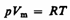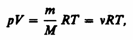Закон Бойля-Мариотта: изучая изотермические процессы, английский ученый Бойль и французский Мариотт не зависимо друг от друга установили закон:
для данной массы газа при постоянной температуре давление газа изменяется обратно пропорционально объему.
pV=const
Закон Гей-Люссака:
Для данной массы газа при постоянном давлении объем газа изменяется линейно с температурой.
V=V0 (1+αt), где V0 – объем газа при 00 С, α – коэффициент объемного расширения газа.
Закон Дальтона.
Пусть в некотором объеме находится смесь газов(воздух), имеющая давление p. Удалим из объема все газы кроме одного например азота. Тогда этот газ будет оказывать давление p1 называемым парциальным давлением. Парциальное давлением называют то давление, которое имел бы этот газ, если бы все остальные газы были бы удалены из объема.
Давление газовой смеси равно сумме парциальных давлений входящих в нее газов:
p=p1+p2+p3+…
Закон Авогадро.
При одинаковых температуре и давлении киломоли любых газов занимают одинаковые объемы.
При нормальных условиях этот объем составляет 22,42 л/моль.
Уравнение Менделеева-Клапейрона:
Состояние некоторой массы газа определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т. Между этими параметрами существует определенная связь, называемая уравнением состояния, которое в общем виде дается выражением

где каждая из переменных является функцией двух других.
Французский физик и инженер Б. Клапейрон (1799—1864) вывел уравнение состояния идеального газа, объединив законы Бойля – Мариотта и Гей-Люссака. Пусть некоторая масса газа занимает объем V 1, имеет давление р 1 и находится при температуре T 1. Эта же масса газа в другом произвольном состоянии характеризуется параметрами р 2, V 2, T 2. В соответствии с законами Бойля — Мариотта и Гей-Люссака запишем:
p1V1=  V2,
V2,
 /p2=T1/T2.
/p2=T1/T2.
Исключив из уравнений и  получим
получим

для данной массы газа величина pV/T остается постоянной, т.е.
pV/T=const=B
Это выражение является уравнением Клапейрона, в котором B — газовая постоянная, различная для разных газов.
Русский ученый Д. И. Менделеев (1834—1907) объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение pV/T=const=B к одному молю, использовав молярный объем V m. Согласно закону Авогадро, при одинаковых р и Т моли всех газов занимают одинаковый молярный объем V m, поэтому постоянная В будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называется газовой постоянной. Уравнению
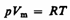
удовлетворяет лишь идеальный газ, и оно является уравнением состояния идеального газа, называемым также уравнением Менделеева-Клапейрона.
Числовое значение молярной газовой постоянной определим полагая, что моль газа находится при нормальных условиях (р 0 = 1,013×105 Па, T 0=273,15 К, V m=22,41×10–3 м3/моль): R =8,31 Дж/(моль×К).
Для моля газа можно перейти к уравнению Менделеева-Клапейрона для произвольной массы газа. Если при некоторых заданных давлении и температуре один моль газа занимает молярный объем V m, то при тех же условиях масса т газа займет объем V= (т/М)V m, где М — молярная масса (масса одного моля вещества). Единица молярной массы — килограмм на моль (кг/моль). Уравнение Менделеева-Клапейрона для массы т газа
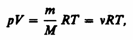




 V2,
V2,