С повышением температуры скорость химического процесса обычно увеличивается. В 1879 г. голландский ученый Я. Вант-Гофф сформулировал эмпирическое правило: с повышением температуры на 10 К скорость большинства химических реакций возрастает в 2-4 раза.
Математическая запись правила Я. Вант-Гоффа:
γ10 = (kт+10)/kТ где kТ - константа скорости реакции при температуре Т; kт+10 - константа скорости реакции при температуре т+10; γ10 - температурный коэффициент Вант-Гоффа. Его значение колеблется от 2 до 4. Для биохимических процессов γ10 изменяется в пределах от 7 до 10.
Все биологические процессы протекают в определенном интервале температур – 45-50 °С. Оптимальной является температура 36-40 °С. В организме теплокровных животных эта температура поддерживается постоянной благодаря терморегуляции соответствующей биосистемы. При изучении биосистем пользуются температурными коэффициентами γ2, γ3, γ5. Для сравнения их приводят к γ10.
Зависимость скорости реакции от температуры, в соответствии с правилом Вант-Гоффа, можно представить уравнением:
V2/V1 = γ ((T2-T1)/10)
Энергия активации.
Значительное возрастание скорости реакции при повышении температуры нельзя объяснить только увеличением числа столкновений между частицами реагирующих веществ, так как, в соответствии с кинетической теорией газов, с возрастанием температуры количество столкновений увеличивается в незначительной степени. Увеличение скорости реакции с повышением температуры объясняется тем, что химическая реакция происходит не при любом столкновении частичек реагирующих веществ, а только при встрече активных частиц, обладающих в момент столкновения необходимым избытком энергии.
Энергия, необходимая для превращения неактивных частичек в активные, называется энергией активации (Eа).
Энергия активации – избыточная, по сравнению со средним значением, энергия, необходимая для вступления реагирующих веществ в реакцию при их столкновении.
Энергию активации измеряют в килоджоулях на моль (кДж/моль). Обычно Е составляет от 40 до 200 кДж/моль.
Энергетическая диаграмма экзотермической и эндотермической реакции представлена на рис. 3. Для любого химического процесса можно выделить начальное, промежуточное и конечное состояния. На вершине энергетического барьера реагенты находятся в промежуточном состоянии, которое называется активированным комплексом, или переходным состоянием. Разность между энергией активированного комплекса и начальной энергией реагентов равна Еа, а разность между энергией продуктов реакции и исходных веществ (реагентов) - ΔН, тепловому эффекту реакции. Энергия активации, в отличие от ΔН, всегда величина положительная. Для экзотермической реакции (рис. 3, а) продукты расположены на более низком энергетическом уровне, чем реагенты (Еа < ΔН).
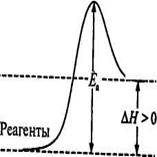

| Рис. 3. Энергетические диаграммы реакций:
А – экзотермической Б - эндотермической
| |
А Б
Еа является основным фактором, определяющим скорость реакции: если Еа > 120 кДж/моль (выше энергетический барьер, меньше активных частиц в системе), реакция идет медленно; и наоборот, если Еа < 40 кДж/моль, реакция осуществляется с большой скоростью.
Для реакций с участием сложных биомолекул следует учитывать тот факт, что в активированном комплексе, образовавшемся при соударении частиц, молекулы должны быть ориентированы в пространстве определенным образом, так как трансформации подвергается лишь реагирующий участок молекулы, небольшой по отношению к ее размеру.
Если известны константы скорости k1 и k2 при температурах Т1 и Т2, можно рассчитать значение Еа.
В биохимических процессах энергия активации в 2-3 раза меньше, чем в неорганических. Вместе с тем Еа реакции с участием чужеродных веществ, ксенобиотиков, значительно превышает Еа обычных биохимических процессов. Этот факт является естественной биозащитой системы от влияния чужеродных веществ, т. е. естественные для организма реакции происходят в благоприятных условиях с низкой Еа, а для чужеродных реакций Еа высокая. Это является генным барьером, характеризующим одну из главных особенностей протекания биохимических процессов.








