Металл - это необходимый материал в промышленности.
Чаще всего в промышленности и строительстве используются не чистые металлы, а их сплавы, в основе которых лежит какой-либо элемент и разнообразные добавки, улучшающие его качества – надежность, прочность и т.д. Самыми распространенными сплавами являются сталь, чугун, а также материалы, в основе которых лежит медь и алюминий.
Сталь является самым востребованным металлом. В большинстве случаев, сталь представляет собой сплав железа с углеродом, количество которого достигает двух процентов. Сплавы стали подразделяются на несколько видов: малоуглеродистые, уровень углерода в которых не превышает 0,25%, высокоуглеродистые с содержанием углерода свыше 0,55% и легированные, дополненные никелем, хромом, ванадием.
Очень большими являются по объему производства чугуна, который также представляет собой сплав железа и углерода. В отличие от стали, количество углерода в чугуне несколько больше. Для придания сплаву прочности в чугун добавляется кремний. Особенно широкое распространение чугун получил в строительстве: он используется для изготовления трубопроводной арматуры, крышек люков и других элементов, основным требованием которых является прочность.
Хотя сплавы из алюминия не так распространены, как материалы, названные выше, некоторые их достоинства делают их незаменимыми для некоторых операций. Прежде всего, сплавы из алюминия отличает экономичность, легкость в обработке и другом использовании, а также легкодоступность. Такие сплавы без труда поддаются ковке, сварке, штампованию и другим подобным операциям, а также хорошо поддаются обработке на металлорежущих станках. Использование алюминиевых сплавов ограничено лишь тем, что при высоких температурах они теряют ряд своих свойств. Так, температура 200 С, уже является для них высокой, а термоустойчивость – это очень важное свойство металла. К достоинствам алюминиевых сплавов относится их безвредность и экологичность, благодаря чему их можно использовать даже для хранения и перевозки пищевых продуктов, стойкость к появлению коррозии, высокая отражательная способность, а также немагнитность.
Наиболее часто алюминиевые сплавы применяются в машиностроении. Кроме этого, они необходимы для создания высоковольтных линий и изготовления некоторых архитектурно-отделочных материалов (3).
Основные классы неорганических соединений
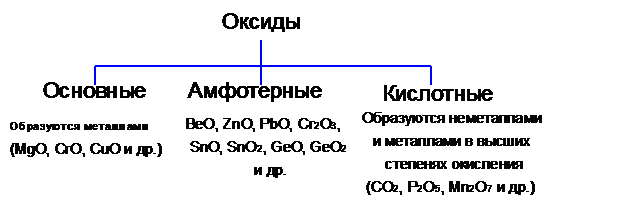
Основнымиоксидами называются такие, которые при взаимодействии с кислотами образуют соль и воду. Соединение этих оксидов с водой относят к классу оснований (например, оксиду Na2O соответствует основание NaOH).
Кислотнымиоксидами называются такие, которые при взаимодействии с основаниями образуют соль и воду. Соединение этих оксидов с водой относят к классу кислот (например, оксиду Р2О5 соответствует кислота Н3РО4, а оксиду Сl2О7 – кислота НСlО4).
Камфотернымоксидами называются такие, которые при взаимодействии с кислотами и основаниями с образованием соли и воды. Соединение этих оксидов с водой могут иметь как кислотные, так и основные свойства (например, амфотерному оксиду ZnO соответствует основание Zn(OH)2 и кислота H2ZnO2).
Характерной особенностью оксидов является способность их к образованию солей. Поэтому такие оксиды относятся к солеобразующим. Наряду с солеобразующими существуют и несолеобразующие, или безразличные, оксиды, которые не образуют солей. Примером могут служить CO, N2O, NO (3)
Химические свойства оксидов
| ОСНОВНЫЕ
| КИСЛОТНЫЕ
|
| 1.Основные оксиды взаимодействуют с кислотами с образованием соли и воды
CuO+H2SO4 → CuSO4+H2O
| 1. Кислотные оксиды взаимодействуют с растворимыми основаниями (щелочами), с образованием соли и воды:
СО2+2NaOH → Na2СО3+ H2O
|
| 2.Оксиды активных металлов взаимодействуют с водой, с образованием щелочи:
Li2O+H2O→ 2LiOH
| 2. Если кислотные оксиды взаимодействуют с водой, то при этом образуются кислоты:
P2O5+3H2O → 2H3PO4
|
| Основные и кислотные оксиды взаимодействуют между собой с образованием соли:
СаО+СО2 → СаСО3.
|
| Амфотерные оксиды взаимодействуют как с кислотами, так и с основаниями с образованием соли и воды:
ZnO+2HCl → ZnCl2+H2O
ZnO+2NaOH → Na2ZnO2+H2O
или ZnO+2NaOH+H2O → Na2[Zn(OH)4]
|
Основания (гидроксиды) -сложные вещества, в состав которых входят атомы металлов (катионов) и одна или несколько гидроксильных групп-Ме(ОН)n.
Число гидроксогрупп в молекуле основания зависит от валентности металла и обычно равно ей. Например, Сu(ОН)2-гидроксид меди (II), Fe(ОН)3-гидроксид железа (III).







