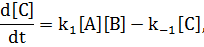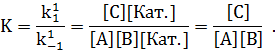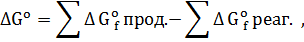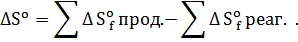Положение равновесия в обратимых химических реакциях характеризуется кинетическими и термодинамическими константами равновесия.
Кинетические константы равновесия выводятся из факта, что в состоянии равновесия концентрации реагентов и продуктов реакции не меняются. Рассмотрим две реакции, одна из которых протекает в отсутствии катализатора, а другая в присутствии катализатора:

Скорости накопления продукта реакции С в этих реакциях могут быть выражены дифференциальными уравнениями:
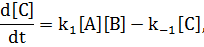

В приведенных уравнениях концентрации являются текущими. При достижении равновесия концентрации в реакционной системе достигают своего равновесного состояния, и далее остаются неизменными. В силу этого первые производные в левой части приведенных выше уравнений становятся равными нулю. Отсюда следует, что:


В данных уравнениях все концентрации уже являются равновесными. Отношение константы скорости прямой реакции к константе скорости обратной реакции получило название кинетической константы равновесия реакции. Кинетические константы равновесия для рассмотренных выше превращений выражаются уравнениями:

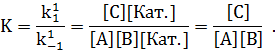
Из приведенных уравнений видно, что кинетические константы равновесия, как в некаталитической, так и в каталитической реакциях, описываются совершенно одинаковыми выражениями. Отсюда следует, что кинетические константы равновесия некаталитических и каталитических реакций равны друг другу. Из этого утверждения следует важное следствие: если катализатор вызывает увеличение константы скорости прямой реакции на какую-либо величину (например, в 104 раз), то на такую же величину возрастает константа скорости обратной реакции (тоже в 104 раз). За счет увеличения скоростей прямой и обратной реакций в каталитических взаимодействиях сокращается время достижения состояния равновесия в реагирующей системе по сравнению с некаталитическими процессами. Однако на величины кинетических констант равновесия катализатор влияния не оказывает.
Термодинамические параметры реакций (стандартные величины свободной энергии Гиббса, энтальпии, энтропии) рассчитываются как разница суммы термодинамических параметров образования продуктов взаимодействия и суммы термодинамических параметров образования реагентов:
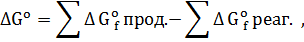

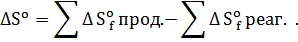
Легко видеть, что для рассмотренных выше модельных превращений все термодинамические параметры для некаталитической и каталитической реакции полностью совпадают друг с другом. Таким образом, как некаталитические, так и каталитические превращения характеризуются совершенно одинаковыми термодинамическими параметрами.
Термодинамическая константа равновесия химической реакции выводится из условия, что при достижении равновесия сумма химических потенциалов продуктов реакции становится сумме химических потенциалов реагентов. Стандартная величина свободной энергии реакции связана с ее константой равновесия уравнением [14]:

Коль стандартные величины свободных энергий некаталитической и каталитической реакций равны друг другу, то отсюда следует, что и термодинамические константы равновесия некаталитической и каталитической реакций совпадают друг с другом.