Установка для электролитического получения хлора и гидроксида калия, вода дистиллированная, хлорид калия, раствор метилового оранжевого, 0,5 н. раствор серной кислоты, пероксид водорода, 1 стакан, мерный цилиндр, коническая колба на 200 мл, бюретка, секундомер, технические весы.
Методика проведения эксперимента
1. Приготовить раствор хлорида калия с концентрацией, заданной преподавателем.
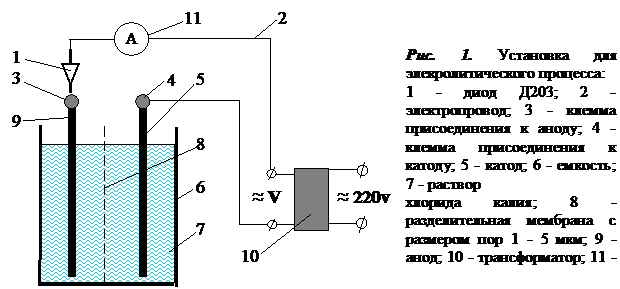
2. Провести электролиз раствора хлорида кадия на установке, представленной на рис. 1, по следующей методике: раствор хлорида калия залить в емкость 6. Убедиться, что установка готова к работе. Установить с помощью трансформатора 10 напряжение (контроль вести за током по амперметру 11), заданное преподавателем. Электролиз вести в течение заданного времени. Постоянно следить за силой тока по амперметру! Затем установку отключить от электрической сети. Перелить анолит и католит в отдельные емкости и замерить их объем.
3. Провести анализ католита на содержание КOH по следующей методике.
Берут пипеткой 20 мл раствора и переносят их в коническую колбу, емкостью 200 мл. Пробу разбавляют дистиллированной водой, прибавляют несколько капель раствора метилового оранжевого и титруют 0,5 н. раствором серной кислоты.
Если метиловый оранжевый от действия гипохлорида калия обесцвечивается, то последний необходимо разрушить несколькими каплями раствора пероксида водорода.
Содержание КOH в растворе (г/л) рассчитывается по формуле:
С КOH =  ,
,
где а − количество миллилитров 0,5 н. раствора кислоты, пошедшего на титрование; 0,056 − количество граммов КOH в 1 мл нормального раствора.
4. Рассчитать катодный выход продукта по току по следующей методике.
Выход по току определяется соотношением:
 ,
,
где m0 − практически полученное количество продукта, г; m − теоретическое количество продукта, которое могло бы выделиться в процессе электролиза, г.
Если через раствор в процессе опыта протекал ток I в продолжении t часов, то m = I . t . ЭВ,
где ЭВ − электрохимический эквивалент вещества (для КОН равен 2,089 г/А.ч).
Полученное количество продукта m0 определяется по концентрации и количеству катодной жидкости:
m0 = C КOH . VK,
где C NaOH − концентрация КOH в католите, г/л; VK − объем раствора в катодном пространстве, л.
Отсюда вычисляется катодный выход.
5. Составить материальный баланс. Для процесса получения щелочи и хлора удобнее всего составить материальный баланс по иону калия. При этом в баланс не вводится материал электродов, количества образующихся газов − хлора, кислорода и т.д. Баланс калия в процессе электролиза составляется по следующей форме:
Таблица
Материальный баланс по иону калия
| Приход
| Расход
|
| Статья прихода
| Кол-во, г
| %
| Статья расхода
| Кол-во, г
| %
|
| КCl
Н2О
|
|
| КOH
КCl
КOCl
КClO3
Н2О
|
|
|
| ИТОГО:
|
|
| ИТОГО:
|
|
|
5
Отчет должен включать в себя следующее:
Титульный лист.
Цель работы.
1. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. Задание
2.2. Приборы, оборудование, материалы.
2.3. Методика проведения эксперимента.
2.4. Экспериментальные данные.
2.5. Обработка экспериментальных данных.
3. ВЫВОД
СПИСОК ИСПОЛЬЗУЕМЫХ ИСТОЧНИКОВ
Контрольные вопросы
1. Что такое электролиз и для чего его применяют?
2. Расскажите о процессе электролиза хлорида калия.
3. Влияет ли концентрация исходного раствора на выход готовых продуктов и каким образом?
4. Каким образом влияют силовые характеристики тока на выход готового продукта?
5. Объясните конструкцию и принцип работы модельной установки электролиза.
6. Каким образом ведут расчет количества компонентов, образовавшихся в результате электролиза раствора.
7. Опишите принцип составления материального баланса.




 ,
, ,
,


